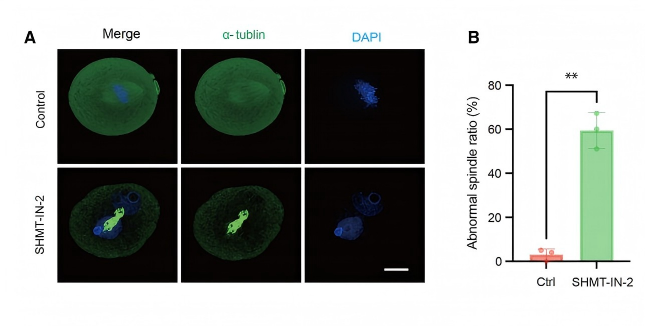
在生命最初的旅程中,一顆受精卵需要經(jīng)歷復(fù)雜而精密的細(xì)胞分裂與分化,才能最終成功著床并發(fā)育為健康的胚胎。然而,不少胚胎在體外培養(yǎng)過程中會(huì)停滯在早期階段,這成為輔助生殖技術(shù)(ART)中一大難題。

腫瘤球體(3D細(xì)胞模型)比傳統(tǒng)2D培養(yǎng)更能模擬真實(shí)腫瘤的微環(huán)境,但其內(nèi)部代謝異質(zhì)性(如外層增殖細(xì)胞與內(nèi)層壞死核心的差異)一直缺乏高精度分析方法。現(xiàn)有方法仍存在局限:要么需要切片樣本并在真空環(huán)境下操作,要么難以實(shí)現(xiàn)對球體內(nèi)細(xì)胞的電離檢測。
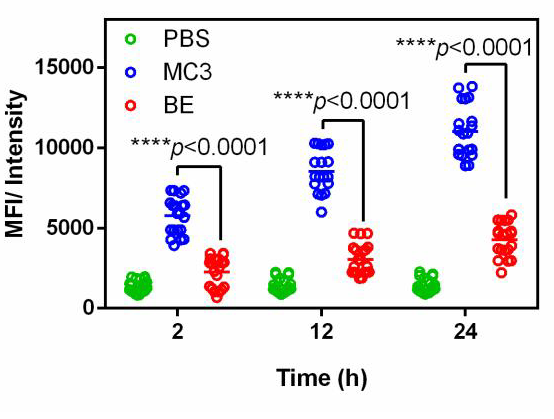
靶向藥物遞送系統(tǒng)(Targeted Drug Delivery Systems, TDDS)指的是通過物理、化學(xué)或生物學(xué)手段,將藥物特異性導(dǎo)向靶組織、靶細(xì)胞甚至胞內(nèi)特定細(xì)胞器的技術(shù)策略。根據(jù)作用機(jī)制的不同,可分為被動(dòng)靶向(Passive Targeting)與主動(dòng)靶向(Active Targeting)。
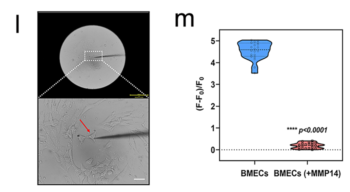
目前針對腦部的主動(dòng)靶向策略完全依賴于配體與血腦屏障(BBB)上特定受體正構(gòu)位點(diǎn)的有效相互作用,而血腦屏障極易受到各種病理生理因素的影響,從而限制了藥物遞送的效率,目前常見挑戰(zhàn)點(diǎn):
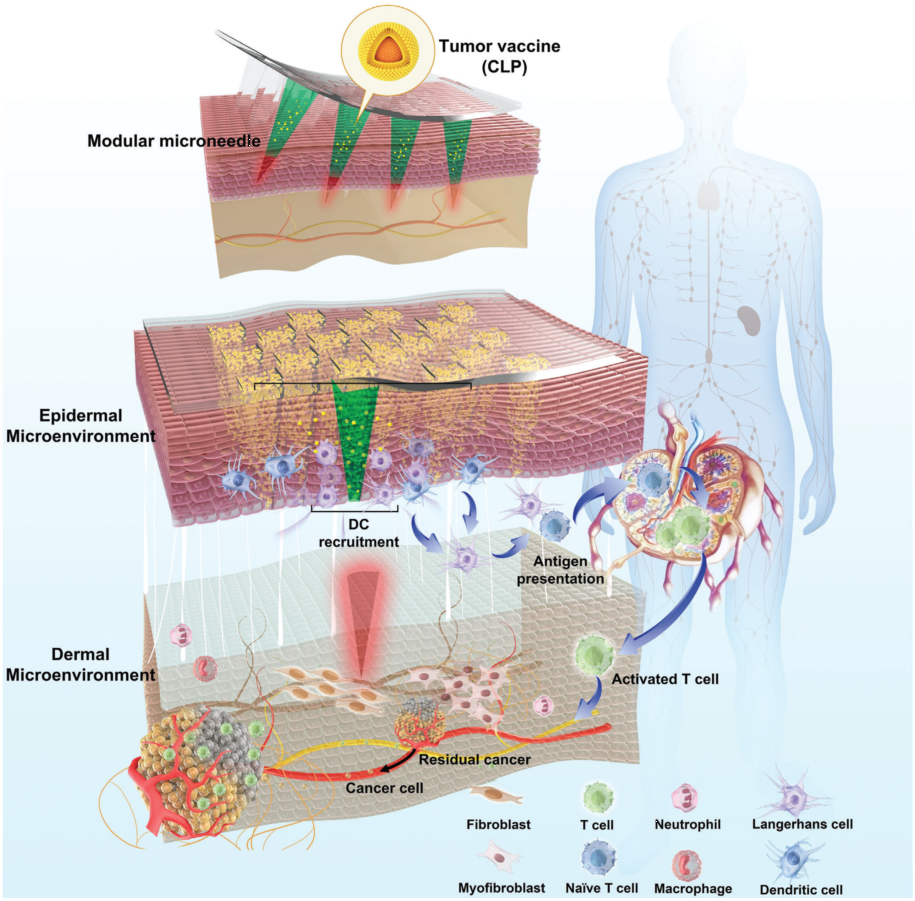
圍手術(shù)期是控制或根除殘留腫瘤、防止其復(fù)發(fā)和轉(zhuǎn)移的獨(dú)特窗口期,充分利用這一關(guān)鍵時(shí)期對充分發(fā)揮免疫治療的潛力至關(guān)重要。因此,有必要通過現(xiàn)有的或新的免疫調(diào)節(jié)方法來減輕術(shù)后傷口微環(huán)境與免疫治療之間的干擾,確保免疫調(diào)節(jié)劑在可耐受和可控的范圍內(nèi)增強(qiáng)免疫治療的效果。
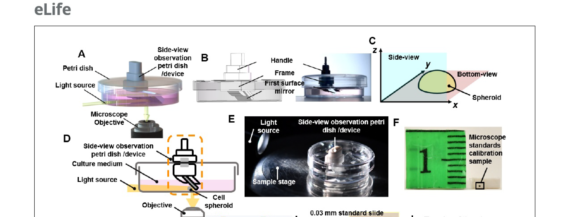
近日,西南大學(xué)余玲教授團(tuán)隊(duì)在eLife發(fā)表文章“Non-destructive in situ monitoring of structural changes of 3D tumor spheroids during the formation, migration, and fusion process”。該團(tuán)隊(duì)通過巧妙的設(shè)計(jì)實(shí)現(xiàn)了從額外的側(cè)向視角觀察3D細(xì)胞球體,從而獲得了比傳統(tǒng)單角度成像更全面的信息。這拓展了以延時(shí)方式研究腫瘤類器官生長或遷移過程中細(xì)胞行為的方法,對該領(lǐng)域具有重要意義。將側(cè)視觀察培
瑞明生物Monicyte活細(xì)胞智能監(jiān)測系統(tǒng),可內(nèi)置于培養(yǎng)箱內(nèi)監(jiān)測活細(xì)胞生長,系統(tǒng)配有強(qiáng)大的AI分析功能,快速合成細(xì)胞生長動(dòng)態(tài)視頻,分析細(xì)胞密度,匯合度,繪制細(xì)胞生長曲線,無人值守監(jiān)測細(xì)胞生長。可應(yīng)用于腫瘤細(xì)胞遷移,神經(jīng)細(xì)胞生長,干細(xì)胞分化,細(xì)胞毒性實(shí)驗(yàn),卵細(xì)胞成熟,類器官生長等細(xì)胞生物學(xué)領(lǐng)域。
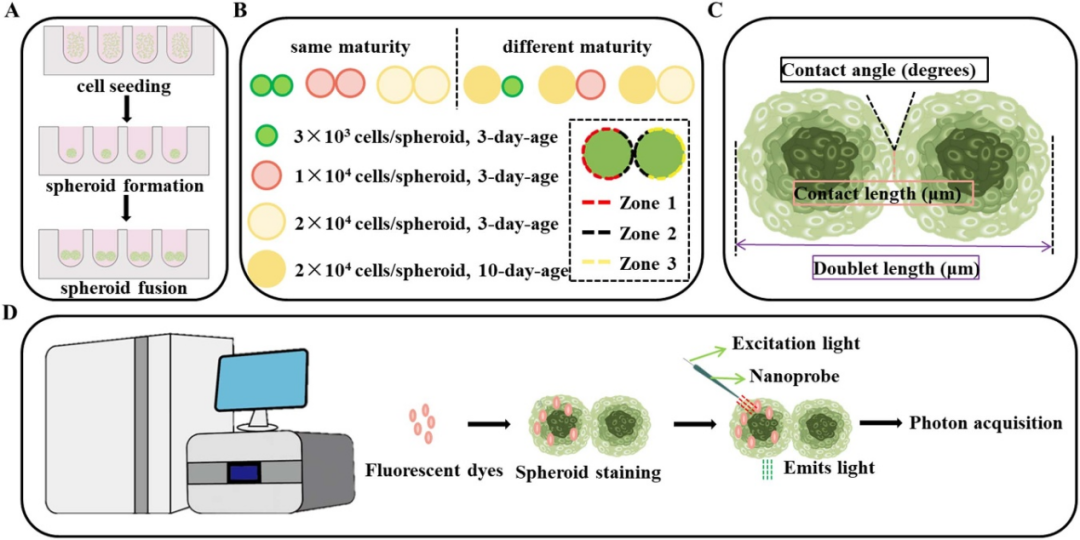
三維細(xì)胞培養(yǎng)由于其獨(dú)特的優(yōu)勢已應(yīng)用于生物學(xué)的許多領(lǐng)域。三維腫瘤球狀體是一種體外自組裝的結(jié)構(gòu),與實(shí)體腫瘤的結(jié)構(gòu)非常相似,在促進(jìn)我們對實(shí)體腫瘤的理解和促進(jìn)更精確的藥物篩選和分析方面具有巨大的潛力。然而,腫瘤球狀體的大小通常在100到500μm之間。它不會(huì)超過1000μm,這不能準(zhǔn)確地反映體內(nèi)實(shí)體腫瘤的物理尺寸。
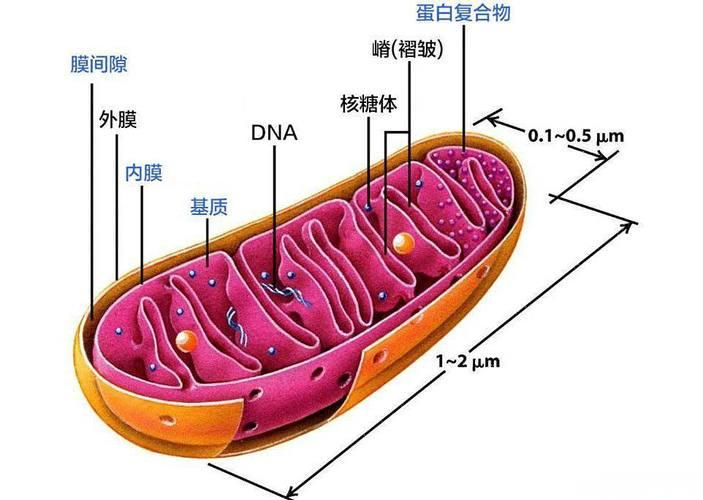
線粒體,一種存在于大多數(shù)真核細(xì)胞中的由兩層膜包被的細(xì)胞器,直徑約0.5~1.0μm,是細(xì)胞中制造能量的結(jié)構(gòu),有氧呼吸的主要場所,是生命科學(xué)領(lǐng)域的熱點(diǎn)研究對象。除為細(xì)胞供能外,線粒體還參與諸如細(xì)胞分化、細(xì)胞信息傳遞和細(xì)胞凋亡等過程,并擁有調(diào)控細(xì)胞生長和細(xì)胞周期的能力。
0510-80328166
 掃一掃,關(guān)注公眾號
掃一掃,關(guān)注公眾號